本文将深入解析制药行业新药临床试验的流程与关键步骤。从临床试验的前期准备到最后的结果分析,每一步都是药品研发过程中至关重要的环节。临床试验作为新药上市的必要步骤,不仅决定了药物的安全性和有效性,还关系到药品能否顺利进入市场并为患者所用。文章将从四个方面详细阐述这一复杂而严谨的过程:临床试验设计、伦理审批和监管要求、患者招募和数据采集、以及数据分析与结果报告。每一环节都要求高标准的执行和严格的科学性,确保最终的临床试验结果具备可信度和科学依据。通过对这些流程与步骤的解析,帮助读者深入了解药品研发的核心步骤,并认识到每个环节在新药上市中的重要性。
1、临床试验设计的核心要素
临床试验设计是新药研发过程中至关重要的第一步。一个良好的临床试验设计能够确保试验的科学性和合理性,为后续的试验结果提供可靠的数据支持。在这一阶段,研发团队需要明确临床试验的目标、对象、研究方法以及预期的研究结果。首先,研究目标需要清晰地定义,是要证明药物的疗效、安全性,还是两者兼备。此外,试验的设计必须选择合适的对照组和实验组,以确保试验结果的科学性和可靠性。
其次,研究方案的制定涉及到多个关键要素。例如,研究的样本量必须足够大,以确保实验结果具备统计学意义。与此同时,研究方法的选择也是设计中的核心环节,通常需要考虑双盲、随机对照等试验方式,以避免偏倚并提高试验的公正性。研究者还需要制定详细的试验时间表、药物给药方案以及安全监测措施,确保每个阶段都能有序进行。
最后,临床试验设计还需要考虑样本的多样性,确保试验人群具有代表性。这意味着研究需要涵盖不同性别、年龄、种族等群体,以便评估药物对不同人群的效果。此外,试验方案的设计还要充分考虑患者的合规性、试验的可操作性以及可能出现的伦理问题。所有这些要素将共同决定试验是否能顺利进行并提供高质量的结果。
九游会(J9)官方网站2、伦理审批与监管要求
在临床试验开始前,药物研发必须遵守相关的伦理审批和监管要求。这是确保患者安全、保护受试者权益的关键步骤。伦理审批通常由医学伦理委员会(Institutional Review Board, IRB)或伦理审查委员会进行。所有新药的临床试验都需要经过该委员会的严格审查,以确保研究方案符合伦理标准,且不会对患者造成不必要的风险。
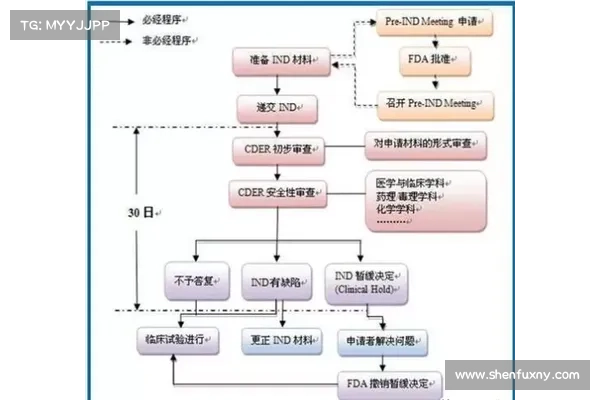
伦理审批的核心内容包括对知情同意的审查,确保患者在自愿的基础上同意参与试验,并完全了解试验的目的、程序、可能的风险和收益等。此外,伦理委员会还会关注临床试验对受试者健康的潜在风险,评估风险与收益的平衡,确保研究设计能够最大程度地降低风险。
与此同时,监管要求方面,不同国家和地区的监管机构(如FDA、EMA、CFDA等)对临床试验有着严格的规定。这些规定包括对试验设计、数据采集、药物使用、受试者选择等各个方面的要求。各个阶段的临床试验都需要通过监管机构的批准才能继续进行。确保所有实验操作都符合这些法律法规,是保证新药试验合规性和有效性的重要保障。
3、患者招募与数据采集
患者招募是临床试验中至关重要的一步,直接关系到试验的样本量和研究结果的准确性。在临床试验的不同阶段,研究者需要根据试验设计招募合适的患者群体。患者招募的过程通常包括招募广告、筛查和知情同意等环节。招募广告通常会发布在医疗机构、网站、报纸等媒体上,目的是吸引符合条件的患者报名参加试验。
在招募患者之后,研究团队会对患者进行严格筛查,以确保其符合试验的纳入标准。这些标准包括年龄、性别、疾病状态、病史等多个方面。只有符合标准的患者才能进入研究,并参与药物的治疗。此外,患者的知情同意书必须在入组前签署,确保患者理解参与试验的目的和可能的风险。
随着临床试验的开展,数据采集也是关键环节。研究者需要严格按照试验方案记录每一位受试者的治疗情况、反应和不良事件,确保数据的完整性和准确性。数据采集不仅包括临床症状的变化,还包括实验室检查数据、影像学资料等。有效的数据采集有助于后期的分析和结论的形成。
4、数据分析与结果报告
临床试验结束后,数据分析是决定药物是否有效及安全的重要环节。数据分析的目的是通过统计学方法,验证药物对患者的影响是否显著,是否满足预定的试验目标。数据分析通常分为描述性统计分析和推断性统计分析两部分。描述性统计分析主要用于描述受试者的基本情况和试验结果的整体趋势,而推断性统计分析则帮助研究者得出结论,判断药物效果的显著性。
此外,数据分析还需要注意统计方法的选择。常用的统计方法包括t检验、卡方检验、回归分析等。研究者需要根据试验的具体目标选择合适的统计方法。值得注意的是,在分析过程中,必须严格遵循盲法原则,避免分析者的偏见影响结果的客观性。
最后,临床试验的结果报告是向监管机构提交的重要文件。报告中需要详细阐述试验的背景、设计、过程、数据分析方法和最终结果。此外,研究者还需要在报告中总结药物的疗效、安全性以及适应症等关键信息。该报告不仅是新药上市申请的基础,也为医学界提供了重要的科研数据。
总结:
通过对新药临床试验流程与关键步骤的详细解析,我们可以看到,临床试验是药品研发中的重要环节,每一个步骤都需严格把控,以确保药物的安全性和有效性。从试验设计到患者招募,再到数据分析与结果报告,每个环节都关乎着药物最终能否成功上市。只有在科学严谨的流程下,才能确保试验数据的可信性和药物的临床价值。
综上所述,制药行业的新药临床试验是一个复杂而高效的过程,涉及到伦理审批、患者招募、数据采集及结果分析等多个环节。每一个步骤的精确执行,都为最终药品的研发和上市奠定了坚实的基础。未来,随着技术的不断进步和法规的日益完善,临床试验的流程将更加高效和透明,助力更多创新药物惠及全球患者。